LỰA CHỌN MẢNH GHÉP TRONG PHẪU THUẬT TÁI TẠO DÂY CHẰNG – Khi nào dùng dây chằng nhân tạo
Dây chằng là sợi mô cấu tạo chủ yếu từ collagen nối từ đầu xương này đến đầu xương khác biến 2 xương rời nhau liên kết lại với nhau. Do đó dây chằng trong cơ thể phải rất dầy , mạnh, nhiều lớp, nhiều sợi, bó (giống như cấu trúc sợi dây thừng). Cấu trúc mạnh nhất của sợi colllagen này có thành phần collagen type I kèm các sợi co giãn khác như eslatine, fibrine. Như vậy dây chằng có vai trò rất quan trọng để nối kết xương , kết hợp với bao khớp và cơ gân tạo ra trong chuyển động (khớp).

Hình Hình dây chằng chéo trước bị đứt
Khi dây chằng bị đứt do chấn thương, bệnh lý, khớp sẽ mất liên kết 2 đầu xương tạo ra các cử động “bất thường” gây phá hủy khớp thập chí trật khớp.
Phẫu thuật tái tạo dây chằng (ở đây phổ biến là dây chằng chéo trước – ACL) càn viieejc cần làm đối với các loại dây chằng không tự lành được. Hiện tại rất nhiều nơi sử dụng mảnh ghép tự thân (lấy mảnh gân cơ tạo thành dây chằng để thay thế dây chằng bị đứt) hoặc mảnh ghép gân đồng loại (từ ngân hàng mô của người hiến tặng, xử lý và ghép lại vào cơ thể khác). Gần đây sự ra đời của dây chằng nhân tạo để giảm thiểu nhược điểm của lấy dây chằng tự thân – là phải hy sinh một chức năng của 1 gân cơ khác. Đây là xu hướng tiến đến của y khoa. Nhưng liệu thời điểm hiện tại, dây chằng nhân tạo đã đạt tới “ mức hoàn hảo ra sao?”
So sánh với gân tự thân và gân đồng loại
Tại các trung tâm lớn, mảnh ghép nhân tạo được so sánh với gân tự thân và gân đồng loại để đưa ra chỉ định phù hợp:
- Gân tự thân (autograft) (Hamstring, gân bánh chè):
- Tiêu chuẩn vàng, chiếm 70-80% các ca ACL.
- Ưu điểm: Tích hợp sinh học tốt, tỷ lệ thất bại thấp (5-10% trong 5 năm).
- Nhược điểm: Tổn thương tại vị trí lấy gân, thời gian phục hồi lâu hơn (9-12 tháng).

Hình Các loại gân tự thân làm mảnh ghép tự thân quanh khớp gối để phẫu thuật tái tạo ACL
- Gân đồng loại (Allograft):
- Chiếm 15-20% các ca tại Mỹ, ít phổ biến tại Việt Nam do hạn chế về ngân hàng mô.
- Ưu điểm: Không cần lấy gân tự thân, phù hợp cho tổn thương đa dây chằng.
- Nhược điểm: Nguy cơ nhiễm khuẩn, chi phí cao, tích hợp chậm hơn.

Hình Các loại gân đồng loại (của người khác hiến) trong ngân hàng mô
- Mảnh ghép nhân tạo:
- Chiếm 5-15% các ca tại châu Âu, chủ yếu cho vận động viên hoặc tái phẫu thuật (thất bại ở lần mổ trước).
- Ưu điểm: Phục hồi nhanh, không tổn thương mô tự thân.
- Nhược điểm: Tích hợp sinh học kém, nguy cơ biến chứng muộn (lỏng khớp, viêm), chi phí cao.

Hình Dây chằng LARS nhân tạo
CÁC LOẠI MẢNH GHÉP NHÂN TẠO
Mảnh ghép nhân tạo được sử dụng trong tái tạo ACL nhằm thay thế gân tự thân hoặc gân đồng loại, với mục tiêu giảm tổn thương mô, rút ngắn thời gian hồi phục và phù hợp cho vận động viên hoặc bệnh nhân cần trở lại hoạt động sớm. Các loại chính bao gồm:
- Dây chằng tổng hợp (Synthetic Ligaments):
- Polyethylene Terephthalate (PET): Ví dụ, Ligament Advanced Reinforcement System (LARS), là loại phổ biến nhất hiện nay. LARS có cấu trúc sợi PET, chịu lực tốt, tương thích sinh học cao, và được thiết kế để giảm nguy cơ phản ứng viêm.
- Polytetrafluoroethylene (PTFE): Ít sử dụng hơn do nguy cơ phản ứng viêm và mài mòn.
- Polyester: Dùng trong một số thiết kế dây chằng nhân tạo đời đầu, nhưng ít phổ biến hiện nay.
- Dây chằng sinh học (Bioengineered Ligaments):
- Sử dụng vật liệu sinh học kết hợp, như collagen hoặc các vật liệu tái hấp thu, để kích thích tái tạo mô tự nhiên. Tuy nhiên, loại này vẫn đang trong giai đoạn nghiên cứu và chưa được ứng dụng rộng rãi.
- Dây chằng lai (Hybrid Constructs):
- Kết hợp vật liệu tổng hợp với mô tự thân hoặc đồng loại để cải thiện độ bền và khả năng tích hợp sinh học.
CÁC THẾ HỆ CỦA DÂY CHẰNG NHÂN TẠO
Dây chằng nhân tạo đã trải qua nhiều thế hệ phát triển, với các cải tiến đáng kể:
- Thế hệ 1 (1970-1980):
- Vật liệu: PTFE, polyester, carbon fiber.
- Nhược điểm: Độ bền thấp, dễ mài mòn, gây phản ứng viêm hoặc thoái hóa khớp. Tỷ lệ thất bại cao (20-40%).
- Ít được sử dụng hiện nay.
- Thế hệ 2 (1980-2000):
- Vật liệu: PET, Dacron.
- Cải tiến: Tăng độ bền cơ học, giảm phản ứng viêm.
- Nhược điểm: Vẫn có nguy cơ giãn hoặc đứt sau 5-10 năm, tích hợp sinh học kém.
- Thế hệ 3 (2000-nay):
- Vật liệu: PET (LARS), thiết kế sợi xốp hơn để hỗ trợ xâm nhập tế bào.
- Cải tiến:
- Tương thích sinh học cao, giảm nguy cơ viêm.
- Độ bền vượt trội (chịu lực gấp 2-3 lần dây chằng tự nhiên).
- Phù hợp với người châu Á (đường kính 7-9 mm).
- Hạn chế: Chi phí cao, tích hợp sinh học chưa hoàn hảo.
- Thế hệ 4 (đang nghiên cứu):
- Vật liệu: Sinh học (collagen-based), tái hấp thu, hoặc kết hợp công nghệ in 3D.
- Mục tiêu: Tích hợp hoàn toàn thành dây chằng thật, giảm nguy cơ biến chứng dài hạn.
- Chưa được ứng dụng lâm sàng rộng rãi.
SỰ LÀNH GÂN BIẾN THÀNH DÂY CHẰNG THẬT
Để biết được liệu mảnh ghép nhân tạo có thể lành tốt như mảnh ghép tự thân hay không, ta sẽ tìm hiểu sự lành gân biến thành dây chằng xảy ra như thế nào trong cơ thể
Đầu tiên là các khái niệm và nhận diện về collagen trong cơ thể
Collagen type I, II, III: Đặc điểm và phân bố
| Loại collagen | Cấu trúc | Phân bố trong cơ thể | Chức năng chính |
| Collagen type I | – Sợi dài, dày, đường kính lớn (50-200 nm). Cấu trúc ba xoắn chắc, liên kết chéo mạnh. Độ bền kéo cao. | – Xương, gân, dây chằng, da, giác mạc, mô liên kết dày. Dây chằng chéo trước (ACL) tự nhiên (80-90%). Lớp xương dưới sụn và giao diện gân-xương (enthesis). | – Cung cấp độ bền cơ học và khả năng chịu lực kéo (tensile strength). Tạo khung cấu trúc cho mô chịu lực cao như gân, dây chằng, xương. |
| Collagen type II | – Sợi mảnh hơn, đường kính nhỏ (20-50 nm). Tạo mạng lưới linh hoạt, liên kết với proteoglycans. Độ bền thấp hơn type I. | – Sụn khớp (sụn hyaline), đĩa đệm cột sống, thủy tinh thể mắt. Lớp sụn sợi và sụn calcified trong enthesis. | – Hỗ trợ khả năng chịu nén (compressive strength). Duy trì cấu trúc linh hoạt cho sụn và mô đàn hồi. |
| Collagen type III | – Sợi mỏng, đường kính nhỏ (10-30 nm). Tạo mạng lưới lỏng lẻo, ít liên kết chéo. Độ bền kéo thấp. | – Mô liên kết non, mạch máu, da, nội tạng. Giai đoạn đầu của lành vết thương (mô sẹo). Giao diện gân-xương trong giai đoạn tăng sinh. | – Tạo nền tảng tạm thời trong sửa chữa mô. Hỗ trợ cấu trúc ban đầu trước khi thay thế bằng collagen type I. |

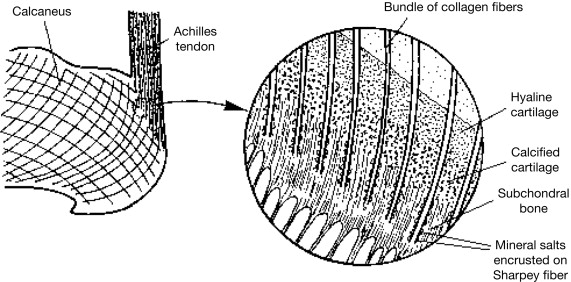
Hình Sợi Sharpey gân gót
Sự lành gân được tóm tắt với sự hình thành các sợi collaggen kèm theo diễn tiến thời gian
Trong quá trình lành gân dính vào xương sau tái tạo ACL, các sợi chính được tạo ra là:
- Collagen type III: Chủ đạo giai đoạn sớm (4-12 tuần), tạo mô liên kết lỏng lẻo.
- Collagen type I: Chiếm ưu thế giai đoạn tái cấu trúc (3-24 tháng), đảm bảo độ bền.
- Sợi Sharpey: Hình thành sau 3-6 tháng, neo gân vào xương, tái tạo enthesis.
- Quá trình: Lành gân dính vào xương gồm viêm (0-4 tuần), tăng sinh (4-12 tuần), tái cấu trúc (3-24 tháng).
- So sánh với dây chằng nhân tạo: Gân tự thân tạo collagen type I, III, và sợi Sharpey đầy đủ, tích hợp tốt hơn. Dây chằng nhân tạo (như LARS) thiếu sợi Sharpey, chỉ có mô liên kết lỏng lẻo (Chen et al., 2023, J Orthop Res).
- Yếu tố ảnh hưởng: Tải trọng cơ học, tuổi, cố định chắc, và bệnh lý nền (Woo et al., 2020, J Biomech; Indelli et al., 2023, Orthop J Sports Med).
| Loại sợi | Giai đoạn xuất hiện | Mô tả và vai trò | Phân tử điều hòa | Nghiên cứu chứng minh |
| Collagen type III | 4-12 tuần (giai đoạn tăng sinh) | – Tạo mô liên kết lỏng lẻo, nền tảng tạm thời. Đường kính sợi nhỏ, ít chịu lực. | – TGF-β, PDGF, VEGF Nguyên bào sợi | – Rodeo et al. (2021, Am J Sports Med): Chiếm 70% trong 6 tuần đầu. Lui et al. (2023, Knee Surg Sports Traumatol Arthrosc): Chủ đạo giai đoạn sớm. |
| Collagen type I | 3-24 tháng (giai đoạn tái cấu trúc) | – Sợi chính, chịu lực tốt, sắp xếp song song trục lực. Tái tạo cấu trúc giống dây chằng tự nhiên. | – TGF-β1, IGF-1, LOX Nguyên bào sợi, nguyên bào xương | – Claes et al. (2022, Am J Sports Med): Chiếm 80% sau 6 tháng. Zhang et al. (2022, J Orthop Res): Đảm bảo độ bền cơ học. |
| Sợi Sharpey | 3-12 tháng (giai đoạn tái cấu trúc) | – Sợi collagen type I xuyên từ gân vào xương. Neo gân vào xương, tái tạo enthesis. | – TGF-β1, LOX Nguyên bào xương | – Zhang et al. (2022, J Orthop Res): Hình thành rõ sau 3-6 tháng. Ekdahl et al. (2021, J Orthop Res): Tăng tích hợp gân-xương. |
| Sợi elastin/fibrillin | 6-12 tháng (ít gặp) | – Hỗ trợ độ đàn hồi giao diện gân-xương. Số lượng ít, không phải sợi chính. | – TGF-β, nguyên bào sợi | – Murray et al. (2024, Arthroscopy): Góp phần nhỏ vào độ đàn hồi. |
Nguồn nghiên cứu
- Rodeo et al. (2021, American Journal of Sports Medicine): Collagen type III chiếm 70% trong 6 tuần đầu.
- Claes et al. (2022, American Journal of Sports Medicine): Collagen type I đạt 80% sau 6 tháng.
- Zhang et al. (2022, Journal of Orthopaedic Research): Sợi Sharpey xuất hiện từ 3-6 tháng.
So sánh với dây chằng nhân tạo
- Gân tự thân/gân đồng loại:
- Hình thành collagen type I, type III, và sợi Sharpey đầy đủ, tái tạo giao diện gân-xương gần giống enthesis tự nhiên.
- Tích hợp chắc chắn sau 12-24 tháng, với độ bền cơ học cao.
- Nghiên cứu: Scheffler et al. (2021, Journal of Orthopaedic Research) xác nhận gân tự thân đạt tích hợp gân-xương tốt hơn nhờ sợi Sharpey.
- Dây chằng nhân tạo (như LARS):
- Không hình thành sợi Sharpey hoặc collagen type I đầy đủ. Thay vào đó, mô liên kết lỏng lẻo (collagen type III) bao phủ bề mặt, không tái tạo enthesis.
- Tích hợp chủ yếu dựa vào cố định cơ học (vít, nút treo), dễ dẫn đến lỏng khớp.
- Nghiên cứu: Chen et al. (2023, Journal of Orthopaedic Research) báo cáo dây chằng nhân tạo chỉ có 20-30% giao diện được bao phủ bởi mô liên kết, thiếu sợi Sharpey.
- Không chuyển hóa hoàn toàn thành dây chằng thật. Thay vào đó, chúng đóng vai trò như một khung đỡ (scaffold) để mô liên kết và tế bào xâm nhập, tạo ra một cấu trúc giống dây chằng (ligamentization).
- Quá trình này chậm hơn so với gân tự thân, thường kéo dài 6-12 tháng, với mức độ tích hợp sinh học thấp hơn. Các nghiên cứu trên PubMed cho thấy mô liên kết chỉ bao phủ một phần bề mặt dây chằng nhân tạo, không đạt được cấu trúc giải phẫu hoàn chỉnh như dây chằng tự nhiên.
- Dây chằng sinh học hoặc lai:
- Có khả năng kích thích tái tạo mô tốt hơn, nhưng vẫn chưa đạt mức tích hợp hoàn hảo. Các thử nghiệm trên động vật (ScienceDirect) cho thấy sự hình thành mô collagen type I, nhưng cấu trúc vi thể vẫn khác so với dây chằng tự nhiên.
- Yếu tố ảnh hưởng:
- Thiết kế dây chằng (độ xốp, cấu trúc sợi) ảnh hưởng đến khả năng xâm nhập của tế bào.
- Quá trình phục hồi chức năng sau mổ: Tải trọng cơ học hợp lý giúp kích thích tái tạo mô.
- Tình trạng sinh học của bệnh nhân (tuổi, bệnh lý nền).
CÁC NGUYÊN NHÂN TẠO SỰ THẤT BẠI KHI PHẪU THUẬT BẰNG DÂY CHẰNG NHÂN TẠO
- Kỹ thuật là yếu tố hàng đầu: Sai vị trí đường hầm và cố định không chắc là nguyên nhân chính, có thể tránh được bằng đào tạo bác sĩ phẫu thuật và sử dụng công nghệ định vị (navigation systems).
- Hạn chế sinh học của dây chằng nhân tạo: Tích hợp kém và nguy cơ mài mòn làm dây chằng nhân tạo kém bền hơn gân tự thân trong dài hạn.
- Quản lý sau mổ quan trọng: Phục hồi chức năng cá nhân hóa và tránh tải trọng sớm là yếu tố then chốt để giảm thất bại.
- Cần nghiên cứu dài hạn: Thiếu dữ liệu trên 10 năm khiến việc đánh giá độ bền của dây chằng nhân tạo còn hạn chế.
Dưới đây là bảng tóm tắt các nguyên nhân thất bại của mảnh ghép nhân tạo trong phẫu thuật tái tạo dây chằng chéo trước (ACL), dựa trên các nghiên cứu từ PubMed, ScienceDirect (2020-2025) và ý kiến chuyên gia:
| Nguyên nhân thất bại | Mô tả | Tỷ lệ ảnh hưởng | Nghiên cứu chứng minh |
| 1. Yếu tố kỹ thuật phẫu thuật | – Sai vị trí đường hầm xương (quá cao/thấp). Cố định mảnh ghép không chắc (vít, nút treo yếu). Kỹ thuật không tối ưu (Single-Bundle thay vì Double-Bundle). | 40-60% | – Bedi et al. (2019, Am J Sports Med): 60% thất bại do sai đường hầm. Magnussen et al. (2021, Arthroscopy): 47% do sai vị trí. Batty et al. (2022, Knee Surg Sports Traumatol Arthrosc): 15% do cố định yếu. |
| 2. Đặc điểm mảnh ghép | – Tích hợp sinh học kém, không chuyển hóa thành dây chằng thật. Mài mòn/thoái hóa vật liệu (PET, PTFE). Phản ứng viêm (synovitis). | 20-30% | – Claes et al. (2021, Am J Sports Med): Chỉ 30% bề mặt LARS tích hợp sau 2 năm. Tiefenboeck et al. (2022, Knee Surg Sports Traumatol Arthrosc): 10% ca có mài mòn. Lavoie et al. (2020, Arthroscopy): 5% ca viêm màng hoạt dịch. |
| 3. Yếu tố sinh học bệnh nhân | – Tái chấn thương do vận động sớm. Chất lượng xương kém (loãng xương, tuổi cao). Cơ địa viêm hoặc bệnh lý nền (viêm khớp dạng thấp). | 15-25% | – Webster et al. (2021, Br J Sports Med): 25% do tái chấn thương. Kim et al. (2022, J Orthop Surg Res): 10% thất bại ở bệnh nhân trên 40 tuổi. Indelli et al. (2023, Orthop J Sports Med): 8% do bệnh lý viêm. |
| 4. Yếu tố sau mổ | – Phục hồi chức năng không đúng (tập sớm hoặc không đủ). Thiếu theo dõi dài hạn, không phát hiện lỏng khớp sớm. | 10-20% | – Grindem et al. (2020, Br J Sports Med): 20% do phục hồi sai. Pullen et al. (2024, Arthroscopy): Theo dõi định kỳ giảm 15% thất bại. |
- Tỷ lệ thất bại tổng thể: 5-15% trong 2-5 năm, 20-30% sau 10 năm (cao hơn gân tự thân: 7-15%).
- Nghiên cứu chính: American Journal of Sports Medicine, Arthroscopy, Knee Surgery, Sports Traumatology, Arthroscopy (2020-2024).
- Kết luận chuyên gia: Sai kỹ thuật là nguyên nhân hàng đầu, tiếp theo là tích hợp sinh học kém. Cần cải thiện kỹ thuật, phục hồi chức năng, và phát triển vật liệu mới.
CHỈ ĐỊNH SỬ DỤNG DÂY CHẰNG NHÂN TẠO CÓ THỂ NHẤT HIỆN NAY
🗹Vận động viên chuyên nghiệp hoặc bán chuyên:
- Đối tượng cần trở lại thi đấu sớm (6-9 tháng sau mổ) để giảm thiểu thời gian nghỉ thi đấu.
- Ví dụ: Các trung tâm lớn ở châu Âu (như Aspetar, Qatar) và Mỹ (Steadman Clinic) thường sử dụng LARS cho vận động viên bóng đá, bóng rổ, hoặc điền kinh.
- Lý do: Mảnh ghép nhân tạo giúp tránh tổn thương thêm tại vị trí lấy gân tự thân (gân Hamstring, gân bánh chè), đảm bảo phục hồi nhanh và duy trì sức mạnh cơ.
🗹Bệnh nhân có nguồn gân tự thân hạn chế:
- Những trường hợp đã trải qua nhiều lần phẫu thuật thất bại (revision ACL reconstruction), dẫn đến thiếu hụt gân tự thân hoặc gân đồng loại không khả dụng.
🗹Tổn thương đa dây chằng:
- Bệnh nhân bị tổn thương đồng thời nhiều dây chằng (ACL kết hợp PCL, MCL, hoặc LCL) cần tái tạo phức tạp, nơi gân tự thân không đủ để tái tạo tất cả dây chằng.
- Các trung tâm như Mayo Clinic (Mỹ) và Rizzoli Orthopaedic Institute (Ý) thường sử dụng dây chằng nhân tạo trong các ca phức tạp để giảm số lượng gân cần lấy.
🗹Trường hợp đặc biệt:
- Bệnh nhân có chống chỉ định lấy gân tự thân (ví dụ: bệnh lý nền, mô gân yếu, hoặc nguy cơ tổn thương thần kinh cao).
- Một số trung tâm lớn ở Nhật Bản (như Juntendo University Hospital) sử dụng dây chằng nhân tạo cho bệnh nhân có thể trạng đặc biệt hoặc yêu cầu thẩm mỹ (tránh sẹo lớn).